中國化妝品新原料管理
新原料定義:在我國境內(nèi)首次使用于化妝品的天然或者人工原料為化妝品新原料。
管理方式:具有防腐、防曬、著色、染發(fā)、祛斑美白功能的化妝品新原料,經(jīng)國務(wù)院藥品監(jiān)督管理部門注冊后方可使用;其他化妝品新原料應(yīng)當(dāng)在使用前向國務(wù)院藥品監(jiān)督管理部門備案。
安全監(jiān)測期:經(jīng)注冊、備案的化妝品新原料投入使用后3年內(nèi),新原料注冊人、備案人應(yīng)當(dāng)每年向國務(wù)院藥品監(jiān)督管理部門報告新原料的使用和安全情況。對存在安全問題的化妝品新原料,由國務(wù)院藥品監(jiān)督管理部門撤銷注冊或者取消備案。3年期滿未發(fā)生安全問題的化妝品新原料,納入國務(wù)院藥品監(jiān)督管理部門制定的已使用的化妝品原料目錄。經(jīng)注冊、備案的化妝品新原料納入已使用的化妝品原料目錄前,仍然按照化妝品新原料進行管理。
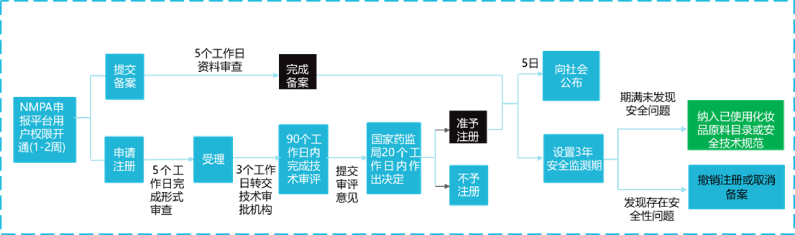
化妝品新原料注冊備案申報流程:
化妝品新原料情形及申報類型
| 化妝品新原料情形 | 申報類型 |
| 情形1:國內(nèi)外首次使用的具有防腐、防曬、著色、染發(fā)、祛斑美白、防脫發(fā)、祛痘、抗皺(物理性抗皺除外)、去屑、除臭功能以及其他國內(nèi)外首次使用的具有較高生物活性的化妝品新原料。 | 新原料注冊 (防腐、防曬、著色、染發(fā)、祛斑美白功能) |
| 新原料備案 (其他功效) |
|
| 情形2:國內(nèi)外首次使用的,不具有防腐、防曬、著色、染發(fā)、祛斑美白、防脫發(fā)、祛痘、抗皺(物理性抗皺除外)、去屑、除臭功能的新原料。 | 新原料備案 |
| 情形3:不具有防腐、防曬、著色、染發(fā)、祛斑美白、防脫發(fā)、祛痘、抗皺(物理性抗皺除外)、去屑、除臭功能的新原料,且能夠提供充分的證據(jù)材料證明該原料在境外上市化妝品中已有三年以上安全使用歷史的 | 新原料備案 |
| 情形4:具有防腐、防曬、著色、染發(fā)、祛斑美白、防脫發(fā)、祛痘、抗皺(物理性抗皺除外)、去屑、除臭功能,且能夠提供充分的證據(jù)材料證明該原料在境外上市化妝品中已有三年以上安全使用歷史的新原料 | 新原料注冊 (防腐、防曬、著色、染發(fā)、祛斑美白功能) |
| 新原料備案 (其他功效) |
|
| 情形5:具有安全食用歷史的化妝品新原料(原料所使用的部位應(yīng)與食用部位一致) | 新原料備案 |
| 情形6:化學(xué)合成的由一種或一種以上結(jié)構(gòu)單元,通過共價鍵連接,平均相對分子質(zhì)量大于1000道爾頓,且相對分子質(zhì)量小于1000道爾頓的低聚體含量少于10%,結(jié)構(gòu)和性質(zhì)穩(wěn)定的聚合物(具有較高生物活性的原料除外) | 新原料備案 |
化妝品新原料情形分類和資料項目要求
| 資料要求 | 情形分類 | ||||||
| 情形1 | 情形2 | 情形3 | 情形4 | 情形5 | 情形6 | ||
| 一、基本信息 | 1.注冊或備案原料信息表 | ○ | ○ | ○ | ○ | ○ | ○ |
| 二、研制報告 | 2.研發(fā)背景 | ○ | ○ | ○ | ○ | ○ | ○ |
| 3.原料基本信息 | ○ | ○ | ○ | ○ | ○ | ○ | |
| 4.原料使用信息① | ○ | ○ | ○ | ○ | ○ | ○ | |
| 5.功能依據(jù)資料 | ○ | ○ | ○ | ○ | ○ | ○ | |
| 6.研制相關(guān)的其他資料 | ○ | ○ | ○ | ○ | ○ | ○ | |
| 三、制備工藝 及質(zhì)量控制標(biāo)準(zhǔn) |
7.制備工藝簡述 | ○ | ○ | ○ | ○ | ○ | ○ |
| 8.穩(wěn)定性試驗數(shù)據(jù) | ○ | ○ | ○ | ○ | ○ | ○ | |
| 9.質(zhì)量規(guī)格指標(biāo)及其檢驗方法 | ○ | ○ | ○ | ○ | ○ | ○ | |
| 10.可能存在的安全性風(fēng)險物質(zhì)及其控制等資料② | |||||||
| 四、安全性評價 | 11.毒理學(xué)安全性評價綜述 | ○ | ○ | ○ | ○ | ○ | ○ |
| 12.急性經(jīng)口或急性經(jīng)皮毒性試驗③ | ○ | ○ | ○ | ○ | |||
| 13.皮膚和眼刺激性/腐蝕性試驗 | ○ | ○ | ○ | ○ | ○ | ○ | |
| 14.皮膚變態(tài)反應(yīng)試驗 | ○ | ○ | ○ | ○ | ○ | ||
| 15.皮膚光毒性試驗④ | |||||||
| 16.皮膚光變態(tài)反應(yīng)試驗⑤ | |||||||
| 17.致突變試驗 | ○ | ○ | ○ | ○ | |||
| 18.亞慢性經(jīng)口或經(jīng)皮毒性試驗 | ○ | ○ | ○ | ||||
| 19.致畸試驗 | ○ | ||||||
| 20.慢性毒性/致癌性結(jié)合試驗 | ○ | ||||||
| 21.吸入毒性試驗⑥ | |||||||
| 22.長期人體試用安全試驗 | ○ | ||||||
| 23.其他毒理學(xué)試驗⑦ | |||||||
| 24.安全性評估報告 | ○ | ○ | ○ | ○ | ○ | ○ | |
| 五、其他資料 | 25.新原料技術(shù)要求 | ○ | ○ | ○ | ○ | ○ | ○ |
| 26.可能有助于化妝品新原料注冊和備案的其他資料⑦ | |||||||
注:上表中畫“○”的,表示必須提交該項資料。資料項目要求的上角標(biāo)注含義解釋如下:
- 對于境外有使用歷史的新原料,應(yīng)說明原料在境外使用于化妝品的情況。
- 可能存在的安全性風(fēng)險物質(zhì)的新原料應(yīng)當(dāng)提交該項資料。
- 在情形3中,能夠同時提供國際權(quán)威安全評價機構(gòu)評價結(jié)論認(rèn)為在化妝品中使用是安全的安全評估報告或符合倫理學(xué)條件下的人體安全性檢驗報告的,可不提交該項資料。
- 原料具有紫外吸收特性時需提交該項試驗資料。
- 除情形6外,原料具有紫外吸收特性時需提交該項試驗資料。
- 原料有可能吸入暴露時須提交該項資料。
- 根據(jù)每個新原料的實際情況提交的其他資料。
化妝品新原料注冊備案檢驗
| 檢驗類型 | 檢驗項目 |
| 質(zhì)量規(guī)格指標(biāo) | 原料性狀(顏色、氣味、狀態(tài)等) 理化性質(zhì)(pH值、溶解度、酸值、粘度、比重等) 定性鑒別方法(化學(xué)結(jié)構(gòu)、成分鑒定) 原料純度或含量 |
| 風(fēng)險物質(zhì)測試 | 微生物(菌落總數(shù)、霉菌和酵母菌總數(shù)、耐熱大腸菌群、金黃色葡萄球菌、銅綠假單胞菌) 重金屬(汞、鉛、砷、鎘) 其他有害物質(zhì)(二噁烷、二甘醇、甲醇、游離甲醛、苯、丙烯酰胺、農(nóng)藥殘留、激素、有害溶劑等) |
| 穩(wěn)定性試驗 | 破壞性試驗 加速試驗 長期保存試驗 |
| 毒理學(xué)試驗 | 1.急性經(jīng)口或急性經(jīng)皮毒性試驗; 2.皮膚和眼刺激性/腐蝕性試驗; 3.皮膚變態(tài)反應(yīng)試驗; 4.皮膚光毒性試驗(原料具有紫外線吸收特性需做該項試驗); 5.皮膚光變態(tài)反應(yīng)試驗(原料具有紫外線吸收特性需做該項試驗); 6.致突變試驗(至少應(yīng)當(dāng)包括一項基因突變試驗和一項染色體畸變試驗); 7.亞慢性經(jīng)口或經(jīng)皮毒性試驗(如果該原料在化妝品中使用經(jīng)口攝入可能性大時,應(yīng)當(dāng)提供亞慢性經(jīng)口毒性試驗); 8.致畸試驗; 9.慢性毒性/致癌性結(jié)合試驗; 10.吸入毒性試驗(原料有可能吸入暴露時須做該項試驗); 11.長期人體試用安全試驗; 12.根據(jù)原料的特性和用途,需提供其他項目的毒理學(xué)試驗資料。 |
| 功效性評價試驗 | 宣稱具有防腐、防曬、祛斑美白、防脫發(fā)、祛痘、抗皺(物理性抗皺除外)、去屑、除臭功能的新原料: 應(yīng)當(dāng)至少包括實驗室研究數(shù)據(jù)或者人體功效性評價試驗資料。 其他功效(滋養(yǎng)、修護、保濕、緊致、舒緩、控油、護發(fā)等)的新原料: 可通過科學(xué)文獻、法規(guī)資料、實驗室研究數(shù)據(jù)或人體功效性評價試驗資料單項或組合的方式,得出申請注冊或進行備案的新原料具有所宣稱功能的明確結(jié)論。 |


